Рак пищевода
– злокачественная опухоль, формирующаяся из разросшегося и переродившегося эпителия стенки пищевода. Клинически рак пищевода проявляется прогрессирующими расстройствами глотания и, как следствие, снижением массы тела в результате недостаточного питания. Первоначально, как правило, обнаруживают опухолевое образование при рентгенографии, эндоскопическом исследовании, КТ или УЗИ. Диагноз — рак пищевода — устанавливают после проведения гистологического исследования биоптата новообразования на предмет обнаружения злокачественных клеток.
Как и всякое злокачественное новообразование, рак пищевода имеет тем более неблагоприятный прогноз, чем позднее выявлено заболевание. Раннее обнаружение рака способствует более выраженному эффекту, опухоли на 3-4 стадии обычно не подлежат полному излечению.
При прорастании раковой опухолью стенок пищевода поражаются окружающие ткани средостения, трахею, бронхи, крупные сосуды, лимфатические узлы. Опухоль склонна к метастазированию в легкие, печень, может распространяться по пищеварительному тракту в желудок и кишечник.
Факторы риска развития рака пищевода
В настоящее время механизмы развития рака пищевода до конца не изучены. Факторами, способствующими возникновению злокачественной опухоли, являются:
- курение;
- злоупотребление алкоголем;
- употребление излишне горячей и слишком холодной пищи;
- производственные вредности (вдыхание токсических газов);
- содержание тяжелых металлов в питьевой воде;
- химические ожоги пищевода при проглатывании едких веществ.
Регулярное вдыхание воздуха, содержащего пылевую взвесь вредных веществ (при проживании в задымленной местности, работе в непроветриваемых помещениях с высокой концентрацией производственной пыли), также может способствовать развитию рака.
Заболеваниями, способствующими развитию рака пищевода, является гастроэзофагеальная болезнь, ожирение, кератодермия. Грыжи пищевода, ахлозия (расслабление нижнего сфинктера пищевода) способствуют регулярному рефлюксу – забросу содержимого желудка в пищевод, что в свою очередь ведет к развитию специфического состояния: болезни Баррета.
Болезнь Баррета (пищевод Баррета) характеризуется перерождением эпителиальной выстилки пищевода по типу желудочного эпителия. Это состояние считают предраковым, как и большинство эпителиальных дисплазий (нарушений развития ткани).
Отмечено, что рак пищевода чаще возникает у лиц старше 45 лет, мужчины страдают им в три раза чаще женщин.
Развитию рака способствует питание, содержащее недостаточное количество овощей, зелени, белка, минералов и витаминов. Нерегулярное питание, склонность к перееданию также оказывают негативное влияние на стенки пищевода, что может способствовать снижению защитных свойств.
Одним из факторов озлокачествления предраковых образований является снижение иммунитета.
Источники
- Zhao H., Misariu AM., Ramirez-GarciaLuna JL., Nobel T., Mueller C., Cools-Lartigue J., Spicer J., Molena D., Bains M., Swisher S., Hofstetter W., Ferri L. Synchronous Esophageal and Lung Cancers — Is Combined Anatomic Resection Appropriate? // Ann Thorac Surg — 2021 — Vol — NNULL — p.; PMID:33905733
- Liao X., Gao Y., Liu J., Tao L., Wang D., Xie D., Mo S. Corrigendum: Combination of Tanshinone IIA and Cisplatin Inhibits Esophageal Cancer by Downregulating NF-κB/COX-2/VEGF Pathway. // Front Oncol — 2021 — Vol11 — NNULL — p.670798; PMID:33905466
- Ali O., Challa SR., Siddiqui OM., Ali S., Kim RE. A rare cause of esophagopleural fistula due to intensity-modulated proton therapy: a case report and review of literature. // Clin J Gastroenterol — 2021 — Vol — NNULL — p.; PMID:33905092
- Xu ZJ., Lin YD. Reply to Zhang et al. // Eur J Cardiothorac Surg — 2021 — Vol — NNULL — p.; PMID:33904932
- Jessen NH., Jensen H., Helsper CW., Falborg AZ., Glerup H., Gronbaek H., Vedsted P. Cancer suspicion, referral to cancer patient pathway and primary care interval: a survey and register study exploring 10 different types of abdominal cancer. // Fam Pract — 2021 — Vol — NNULL — p.; PMID:33904928
- Zhang X., Jiang Y., Zhang L. Nodal skip metastasis in oesophageal cancer: different definition and different prognostic role. // Eur J Cardiothorac Surg — 2021 — Vol — NNULL — p.; PMID:33904927
- Odze R., Spechler SJ., Podgaetz E., Nguyen A., Konda V., Souza RF. Histologic Study of the Esophagogastric Junction of Organ Donors Reveals Novel Glandular Structures in Normal Esophageal and Gastric Mucosae. // Clin Transl Gastroenterol — 2021 — Vol12 — N5 — p.e00346; PMID:33904522
- Conio M., Filiberti RA., Siersema PD., Manta R., Blanchi S., De Ceglie A. A new designed self-expandable metal stent for the management of benign radiotherapy-induced hypopharyngeal or cervical esophageal strictures. // Surg Endosc — 2021 — Vol — NNULL — p.; PMID:33903933
- Davern M., Donlon NE., Power R., Hayes C., King R., Dunne MR., Reynolds JV. The tumour immune microenvironment in oesophageal cancer. // Br J Cancer — 2021 — Vol — NNULL — p.; PMID:33903730
- Lan T., Xue X., Dunmall LC., Miao J., Wang Y. Patient-derived xenograft: a developing tool for screening biomarkers and potential therapeutic targets for human esophageal cancers. // Aging (Albany NY) — 2021 — Vol13 — NNULL — p.; PMID:33903283
Классификация рака пищевода
Рак пищевода классифицируется согласно международной номенклатуре TNM для злокачественных новообразований:
- по стадии (Т0 – предрак, карцинома, неинвазивная эпителиальная опухоль, Т1 – рак поражает слизистую, Т2 — опухоль прорастает в подслизистый слой, Т3 – поражены слои вплоть до мышечного, Т4 – проникновение опухоли сквозь все слои стенки пищевода в окружающие ткани);
- по распространению метастазов в региональных лимфоузлах (N0 – нет метастазов, N1 – есть метастазы);
- по распространению метастазов в отдаленных органах (М1 – есть, М0 – нет метастазов).
Также рак может классифицироваться по стадиям от первой до четвертой в зависимости от распространенности опухоли в стенке и ее метастазирования.
В настоящее время рак пищевода, несмотря на сравнительно невысокие показатели заболеваемости (2,4% у мужчин и 0,6% у женщин), занимает восьмое место в структуре смертности от онкопатологии в РФ [1]. Плоскоклеточный рак пищевода является наиболее распространенным гистологическим типом с чрезвычайно злокачественным характером течения и ранним метастазированием.
К сожалению, более 75% случаев рака пищевода диагностируется только на II—III стадии заболевания, а пятилетняя выживаемость пациентов крайне низкая и варьирует от 4 до 25% [2]. Индекс агрессивности, вычисляемый как соотношение умерших к вновь заболевшим, при раке пищевода крайне высок и составляет около 95% [3]. Поэтому диагностика рака пищевода на ранних стадиях и адекватное лечение могут привести к повышению выживаемости и уменьшению смертности.
Эндоскопическая диагностика раннего рака пищевода и дисплазии высокой степени является сложной задачей современной эндоскопии. Рутинное эндоскопическое исследование в белом свете имеет низкую диагностическую эффективность ввиду трудности выявления минимальных признаков ранних неопластических изменений. Хромоэндоскопия с раствором Люголя является «золотым стандартом» диагностики раннего рака пищевода. Для этого используется 20—50 мл 2—3% раствора Люголя, который представляет собой абсорбирующий краситель, содержащий калиевый йод и чистый йод, который реагирует с некератинизированными эпителиальными клетками, содержащими гликоген [4]. При нанесении раствора Люголя нормальная слизистая пищевода принимает темно-коричневый или зеленовато-коричневый цвет, а области, не содержащие гликоген (неопластические и диспластические участки, цилиндрический эпителий, в ряде случаев — воспалительные изменения), не окрашиваются. В отличие от воспалительных изменений, в случае рака пищевода цвет непрокрашенного при хромоскопии участка может меняться: непосредственно после окраски он имеет желтый цвет, а через 2—3 мин становится розовым. Феномен появления розового цвета («pink color sign») возникает из-за полного отсутствия гликогена в клетках плоскоклеточного рака, что демонстрирует высокую чувствительность и специфичность (88 и 95% соответственно) в диагностике рака пищевода. Однако использование раствора Люголя сопряжено с некоторыми побочными действиями, такими как боль в грудной клетке, кашель и аллергические реакции.
Применение оптических технологий, таких как узкоспектральная эндоскопия, позволило упростить и задачу поиска подозрительных в отношении дисплазии и рака участков, а исследование сделать более безопасным и быстрым. Обнаружение «коричневатых областей» («brownish areas») слизистой оболочки пищевода является специфичным для раннего рака пищевода и обусловлено наличием расширенных нерегулярных сосудов на коричневом фоне. Это позволяет не только выявить раннюю форму рака, но и точно определить его границы. Более того, иногда совместное использование хромоскопии с раствором Люголя и узкоспектральной эндоскопии выявляет феномен металлического серебряного цвета («metallic silver sign») в непрокрашенных при хромоскопии областях неоплазии.
Однако одной из самых эффективных методик диагностики является увеличительная эндоскопия, позволяющая подробно оценить морфологию интрапапиллярных капиллярных петель (inrapapillary capillary loops — ICPLs). Согласно наиболее распространенной классификации Inoue и соавт. [5], по характеристикам капиллярных петель можно не только прогнозировать гистологическое строение участка и различать доброкачественные и злокачественные участки, но и диагностировать уровень инвазии неоплазии и, как следствие, выбирать тактику лечения (см. рисунок) . В соответствии с этой классификацией выделяется пять основных типов интрапапиллярных капиллярных петель, позволяющих детально охарактеризовать изменения плоского эпителия пищевода от нормальной (тип I) слизистой оболочки до плоскоклеточного рака (тип V). Неопластические изменения характеризуются наличием четырех главных изменений капиллярных петель: расширение, извитость, изменения калибра и различие по форме. Наличие одного—двух признаков (в основном заключающихся в удлинении петель) в окрасившемся при хромоскопии участке соответствует II типу и встречается при воспалительных изменениях, в частности при гастроэзофагеальной рефлюксной болезни. Отсутствие изменений капиллярных петель в непрокрасившейся области соответствует типу III и определяет пограничное состояние, которое может включать в себя как воспаление, так и дисплазию низкой степени. Тип IV имеет три из четырех характеристик неоплазии и является маркером дисплазии высокой степени. Интрапапиллярные капиллярные петли типа V также могут различаются выраженностью нерегулярности и деструкции, что кореллирует со степенью инвазии (V1 — инвазия m1, V2 — инвазия m2, V3 — инвазия m3 и sm1, Vn — инвазия sm2 и глубже). M. Arima и соавт. [6] предложили дополнительную характеристику рака пищевода — наличие так называемой аваскулярной зоны, протяженность которой строго соотносится с глубиной инвазии. Однако, помимо изменения капиллярных петель, другим важным признаком является изменение цвета фона слизистой оболочки (области между микрососудами). В зоне неоплазии цвет фона слизистой оболочки отличается (становится темнее) по сравнению с окружающей неизмененной тканью. Это обусловлено наличием экстраваскулярного гемоглобина непосредственно в цитозоле клеток опухоли [7], а также истончением кератинового слоя слизистой оболочки [8].
Типы рисунков интрапапиллярных капиллярных петель по H. Inoue (адаптировано из [5]). а — тип I, нормальная слизистая оболочка; б — тип II, воспалительные изменения; в — тип III, пограничное состояние, требуется наблюдение; г — тип IV, дисплазия высокой степени или рак in situ, требуется эндоскопическая резекция; д — тип V1 (расширение, извитость, изменения калибра и различие по форме), плоскоклеточный рак, степень инвазии m1, абсолютно показана эндоскопическая резекция/диссекция; е — тип V2 (удлинение петель типа V1), плоскоклеточный рак, степень инвазии m2, абсолютно показана эндоскопическая резекция/диссекция; ж — тип V3 (значительное разрушение капиллярного рисунка), плоскоклеточный рак, степень инвазии m3 или sm1, относительно показана эндоскопическая резекция/диссекция; з — тип Vn (формирование новых опухолевых сосудов), плоскоклеточный рак, степень инвазии sm2 и глубже, показано хирургическое лечение.
Выявление раннего рака пищевода или дисплазии высокой степени позволяет провести малоинвазивное эндоскопическое лечение, которое показывает высокую эффективность при длительном наблюдении. По данным Японского общества заболеваний пищевода, пятилетняя выживаемость пациентов с ранним раком пищевода с уровнем инвазии m1 и m2 без метастазов в региональные лимфатические узлы после эндоскопической резекции достигает 95% [9]. Похожие показатели демонстрирует исследование, проведенное в Германии, по данным которого семилетняя выживаемость пациентов с дисплазией высокой степени и ранним плоскоклеточным раком после эндоскопической резекции составила 77% [10]. В настоящее время методикой выбора при ранних неопластических процессах является диссекция в подслизистом слое, поскольку только с помощью этой методики возможно удалить опухоль единым блоком [11]. Показанием для эндоскопической диссекции в подслизистом слое является ранний плоскоклеточный рак, прорастающий до уровня мышечной пластинки слизистой оболочки (mm) и даже инвазирующий в поверхностные слои подслизистого слоя (менее чем на 200 мкм — sm1) [12]. Однако диссекция в подслизистом слое при раннем раке пищевода имеет ряд трудностей и особенностей. Во-первых, методика диссекции в подслизистом слое в пищеводе трудоемка и требует от врача-эндоскописта большого опыта проведения эндоскопических резекций. Сложность операций обусловлена относительно узким просветом пищевода, а также передаточными движениями от близлежащих органов (дыхательные движения и пульсация сердца), что ограничивает возможности манипуляций. Во-вторых, такие осложнения, как перфорация встречаются немного чаще, чем, например, при диссекции в желудке и могут быть причиной пневмомедиатинума и подкожной эмфиземы. Это связано с тем, что стенка пищевода гораздо тоньше стенки желудка. К тому же довольно часто, более чем в половине случаев, пневмомедиастинум диагностируется при повреждении мышечного слоя пищевода даже в отсутствие перфорации, что, однако, не ведет к жизнеугрожающим осложнениям. В-третьих, при удалении патологического участка, распространяющегося более чем на 2/3 окружности пищевода, в зоне операции часто формируются стриктуры, для профилактики которых в этих случаях показано применение преднизолона per os
в постоперационном периоде [13].
С другой стороны, существует несколько особенностей методики эндоскопической диссекции в пищеводе, связанных с особенностями подслизистого слоя, что упрощает проведение операции на некоторых этапах. Подслизистый слой пищевода практически не содержит крупных сосудов, что существенно облегчает гемостаз на этапе диссекции, а инъекция физиологического раствора проводится без существенных усилий и осложнений. Более того, патологический участок локализуется, как правило, в тангенциальном направлении, поэтому подслизистый слой пищевода легко распознать и впоследствии отделить его от мышечного слоя.
Таким образом, применение современных эндоскопических технологий позволяет не только диагностировать самые ранние формы рака пищевода, но и эффективно лечить выявленные образования, а широкое использование этих методик в клинической практике может привести к повышению выживаемости и уменьшению смертности от рака пищевода.
Симптомы рака пищевода
Рак пищевода ранних стадий чаще всего не проявляется клинически, симптоматика начинает проявляться при наличии уже довольно крупной опухоли, мешающей продвижению пищи.
Самым распространенным симптомом рака пищевода является расстройство глотания – дисфагия. Больные стремятся принимать жидкую пищу, более твердая застревает в пищеводе, создавая ощущение «комка» за грудиной.
При прогрессировании опухоли может отмечаться болезненность за грудиной, в глотке. Боль может отдавать в верхнюю часть спины.
Снижение проходимости пищевода способствует возникновению рвоты.
Как правило, продолжительный недостаток питания (связанный с затрудненным приемом пищи) приводит к общей дистрофии: снижению массы тела, расстройству работы органов и систем.
Часто рак пищевода сопровождается постоянным сухим кашлем (возникает рефлекторно как следствие раздражения трахеи), охриплостью (хронический ларингит). На терминальных стадиях развития опухоли в рвоте и кашле можно обнаружить кровь.
Все клинические проявления рака пищевода неспецифичны, но требуют безотлагательного обращения к врачу.
Регулярного диспансерного наблюдения у гастроэнтеролога требуют больные, страдающие болезнью Баррета, как лица с высоким риском развития рака пищевода.
Симптомы
Начальные стадии рака пищевода протекают без симптомов. Проявляется заболевание только тогда, когда происходит нарушение процесса проглатывания и продвижения пищи по пищеводу. Это нарушение возникает при частичном перекрытии просвета пищевода растущей внутрь опухолью. Наличие небольшой опухоли может вызывать спазм стенки и, как следствие, поперхивание едой. При дальнейшем росте новообразования и перекрытии им большей части просвета пищевода больной может потерять способность к нормальному питанию, которое без специальных мероприятий приводит к истощению организма. Задержка пищи выше места сужения приводит к возникновению пищеводной рвоты, срыгиванию слюной и слизью.
Боль невысокой интенсивности за грудиной с иррадиацией в межлопаточную область при прохождении пищи и/или слюнотечение являются поздними симптомами и часто связаны с сопутствующим эзофагитом или прорастанием опухоли в соседние органы. При локализации рака в зоне кардии (перехода пищевода в желудок) первым признаком может быть не нарушение проглатывания и продвижения пищи, а постоянное срыгивание воздуха.
При росте опухоли за пределы пищевода она может сдавливать дыхательные пути с нарушением дыхания. Она также может сдавливать или прорастать в нервные стволы, располагающиеся рядом со стенкой пищевода, приводя к осиплости голоса, кашлю, развитию синдрома Горнера (опущение верхнего века, сужение зрачка, ослабление реакции зрачка на свет, расширение сосудов конъюнктивы глаза, западение глазного яблока, нарушение потоотделения на лице и покраснение кожи лица).
Болезни со сходными симптомами
При глотания (дисфагия), но эти нарушения имеют тенденцию к прогрессированию, хотя и очень медленному. Данное состояние также сопровождают ночной кашель, регургитация (движение в обратном направлении) или аспирация (вдыхание) пищевых масс, иногда повышенное выделение слизи при срыгивании, что связано с застоем в пищеводе. Периодическое возникновение нарушений глотания во время болевого приступа за грудиной свидетельствует в пользу спазма пищевода. Дисфагия сопровождает и раннюю стадию поражения пищевода при склеродермии, но при этом развивается рефлюкс (забрасывание) содержимого желудка в пищевод. Кроме того, дополнительными признаками склеродермии могут быть истончение кожи с просвечиванием подкожных сосудов, уменьшение амплитуды дыхательных движений.
Диагностика рака пищевода
Как всякое новообразование, опухоль пищевода можно назвать злокачественной только после проведения биопсии и выявления раковых клеток. Для визуализации опухоли применяются:
- рентгенография легких (иногда можно увидеть формирование очагов рака в легких и средостении);
- контрастная рентгенография с барием позволяет обнаружить опухолевое образование на стенках пищевода.
Эндоскопическое исследование (эзофагоскопия) позволяет детально осмотреть внутреннюю стенку, слизистую, обнаружить новообразование, исследовать его размер, форму, поверхность, наличие или отсутствие изъязвлений, некротизированных участков, кровоточивости. При эндоскопическом ультразвуковом исследовании можно определить глубину прорастания опухоли в стенку пищевода и окружающие ткани и органы. УЗИ брюшной полости дает информацию о наличие метастазов рака пищевода. МСКТ и магнитно-резонансная томография позволяют получить детальные снимки внутренних органов, выявить изменения лимфоузлов, органов средостения, состояние сосудов и прилегающих тканей.
Позитронно-эмиссионная томография (ПЭТ) дополняет эти исследования, выявляя злокачественные ткани.
При лабораторном исследовании крови определяется присутствие онкомаркеров.
Диагностика
Если симптомы присутствуют, врач начнет специальное рентгенологическое исследование, так называемую ласточку бария. В этом экзамене пациент пьет жидкость, содержащую барий. Это позволяет пищеводу хорошо отображаться на рентгеновском изображении.
Врач также может использовать эзофагоскоп (тонкую гибкую трубку с передней подсветкой) для осмотра внутренних стенок пищевода. Это исследование называется эзофагоскопией. В этом экзамене эзофагоскоп вводится через рот и горло в пищевод. Перед обследованием в область горла распыляется местный анестетик (вещество, вызывающее временную местную анестезию), чтобы пациент не чувствовал боли.
Если лечащий врач обнаруживает ткань, которая не выглядит нормальной, он может взять небольшой кусочек, чтобы исследовать ее под микроскопом на предмет изменений. Этот процесс называется биопсией. Биопсия обычно проводится во время эзофагоскопии, при этом местная анестезия все еще действует, поэтому боли не возникает.
Лечение рака пищевода
Тактика лечения рака пищевода зависит от его локализации, размера, степени инфильтрации стенки пищевода и окружающих тканей опухолью, наличием или отсутствием метастазов в лимфоузлах и других органах, общего состояния организма.
Как правило, в выборе терапии принимает участие несколько специалистов: гастроэнтеролог, онколог, хирург, специалист по лучевой терапии.
В большинстве случаев комбинируют все три основных методики лечения злокачественных новообразований: хирургическое удаление опухоли и пораженных тканей, радио-лучевая терапия и химиотерапия.
Хирургическое лечение рака пищевода заключается в резекции части пищевода с опухолью и прилежащими тканями, удаление располагающихся рядом лимфатических узлов. После чего оставшийся участок пищевода соединяют с желудком. При этом для пластики пищевода могут использовать как ткань самого желудка, так и кишечную трубку. Если опухоль не подлежит полному удалению, то ее иссекают частично, чтобы освободить просвет пищевода.
В послеоперационном периоде пациенты питаются парентерально, пока не восстановится возможность употреблять пищу обычным способом. Для предупреждения развития инфекции в послеоперационном периоде больным назначают антибиотикотерапию. Для уничтожения оставшихся злокачественных клеток дополнительно возможно проведение курса лучевой терапии.
Лучевая противораковая терапия заключается в облучении пораженного участка тела рентгеновским излучением высокой интенсивности. Существует внешняя радиационная терапия (облучение проводят из внешнего источника в область проекции облучаемого органа) и внутренняя радиотерапия (облучение введенными в организм радиоактивными имплантантами).
Нередко лучевая терапия становится методикой выбора при невозможности осуществления хирургического удаления опухоли.
Химиотерапия при раке пищевода применяется в качестве вспомогательного метода подавления активности раковых клеток. Химиотерапию проводят с помощью сильных цитотоксических препаратов.
Больным, которым невозможно произвести хирургическую коррекцию просвета пищевода, с целью облегчения глотания показана фотодинамическая терапия. Эта методика заключается в ведении в опухолевую ткань светочувствительного вещества, после чего воздействуют на рак лазером, разрушая его. Однако добиться с помощью этой методики полного уничтожения злокачественного образования нельзя – это паллиативная терапия.
По окончании курса противоопухолевого лечения все больные обязательно находятся на онкологическом учете и регулярно проходят комплексное обследование.
Причины ↑
Нередкой причиной возникновения плоскоклеточной формы рака являются предраковые заболевания, которым небыли оказано должное внимание и последующее лечение. К таким патологиям относят:
- лейкоплакия — процесс формирования болезни происходит путём ороговевания клеток эпителия глотки, приобретая вид белых бляшек с серым налётом. Визуально больной может не замечать изменений, но ощущать дискомфорт в виде чувства инородного тела в горле. Пятна не возвышаются над поверхностью слизистой глотки, а их размеры варьируются в пределах шести миллиметров;
- пахидермия отличается возникновением наростов на слизистой глотки в результате длительного воспалительного процесса в ней, без должного лечения. Наросты могут иметь как множественный, так и одиночный характер. Из главных признаков болезни определяют охриплость голоса;
- папилломатоз гортани имеет вид сосочкообразных наростов в глотке, имеющие разные степени ороговевания, а после их удаления частые рецидивы. Симптоматика папиллом зависит от места их локализации. При дислокации в области голосовых связок наблюдается хриплость голоса, иногда афония. Если папилломы локализовались в надскладочном пространстве, пациенты отмечают чувство наличия инородного тела в глотке, под голосовыми связками — чувство першения, покашливания и иногда при распространённом процессе затруднение в дыхании. Папилломы подлежат удалению в обязательном порядке.
Лейкоплакия, папилломатоз и пахидермия — это те болезни, которые имеют высокую степень озлокачевания, их также называют облигатными патологиями. При их выявлении следует незамедлительно заниматься вопросом терапии.
Также существую факультативные болезни, которые имеют меньшую степень возможного озлокачивания, но теоретически без предпринятых мер всё же этот факт остаётся не исключен. К таким болезням относят:
- онтактные гранулемы;
- рубцовые образования после хронического течения специфичных инфекций;
- дисплазия слизистой эпителия;
- контактные фибромы.
Помимо предраковых болезней, которые могут переродиться в плоскоклеточный рак гортани, существуют ещё факторы провоцирующие развитие онкологии в области глотки. Наиболее опасными является курение и употребление спиртных напитков. Их канцерогенные вещества повреждают целостность слизистой оболочки глотки, истощая её и приводя к развитию серьёзных мутационных процессов. Также на ряду с приёмом алкоголя и курением опасность вызывает работа на химических предприятиях, лакокрасочной промышленности и по производству тяжёлых металлов, помимо этого проживание в запыленных городах.
Осложнения рака пищевода и его лечения
Основное осложнение рака пищевода – это похудание, возникающее в результате прогрессирующей дисфагии. Также могут возникать различные алиментарные расстройства (алиментарная дистрофия, гиповитаминоз) как следствие недостаточности питания. Злокачественная опухоль может осложняться присоединением бактериальной инфекции. Помимо этого, опухоль может изъязвляться и кровоточить.
Химиотерапия зачастую сопровождается выраженными побочными эффектами: облысение (алопеция), тошнота и рвота, диарея, общая слабость, головные боли.
Пациенты, которым проводилась фотодинамическая терапия, должны избегать прямых солнечных лучей в ближайшие месяцы, поскольку их кожа приобретает особую чувствительность к свету.
Прогноз при раке пищевода
Излечение рака пищевода возможно на ранних стадиях, когда злокачественный процесс ограничен стенкой пищевода. В таких случаях хирургическое иссечение опухоли в сочетании с радио-лучевой терапией дает весьма положительный эффект, есть все шансы к полному выздоровлению.
Когда рак обнаружен уже на стадии метастазирования и опухоль прорастает в глубокие слои, прогноз неблагоприятный, полное излечение, как правило, невозможно.
В тяжелых случаях, старческом возрасте и при невозможности полного удаления опухоли применяют паллиативное лечение для восстановления нормального питания. Выживаемость пациентов с неоперированным раком пищевода не превышает 5%.
Для иностранных граждан мы предлагаем предварительную бесплатную консультацию
Ведущие специалисты Центра ответят на ваши вопросы.
Получить консультацию
Рак пищевода – это злокачественное заболевание, при котором в тканях пищевода появляются опухолевые клетки.
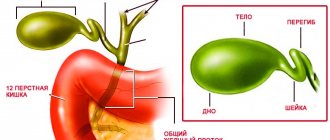
Пищевод – это полая мышечная трубка, по которой твердая и жидкая пища поступают из горла в желудок.
Стенка пищевода состоит из нескольких слоев ткани, а именно:
- слизистого;
- мышечного;
- соединительнотканного.
Рак пищевода, как правило, начинает свое развитие с внутренней слизистой оболочки и в процессе роста распространяется на другие слои. Желудок и пищевод относятся к верхним отделам пищеварительного тракта.