Гастроинтестинальная стромальные опухоли (GIST-ГИСО) встречаются достаточно редко (от 15 до 20 случаев на миллион человек).
Наиболее часто стромальные опухоли появляются в желудке (около семидесяти процентов всех случаев), реже в тонкой кишке, двенадцатиперстной кишке, толстом и прямом кишечнике, пищеводе.
ГИСО-опухоли могут развиваться независимо от возраста, однако примерно в семидесяти пяти процентах случаев они обнаруживаются у пациентов старше пятидесяти лет. У детей стромальные опухоли встречаются весьма редко.
Симптоматика заболевания
У большинства пациентов ГИСО обнаруживаются случайно в рамках рутинных обследований (гастроскопии или колоноскопии, компьютерной томографии или во время операции), т. к. в течение длительного времени не вызывают каких-либо жалоб.
Как правило, первые симптомы появляются, когда уже достаточно крупная опухоль начинает сдавливать прилегающие органы и ткани, однако и эти жалобы являются неспецифичными и могут иметь совершенно другую, неопухолевую, причину. Тем не менее при возникновении любых жалоб, сохраняющихся в течение длительного времени, следует обратиться к специалисту для прохождения диагностики в Германии и уточнения диагноза.
К основным симптомам гастроинтестинальных стромальных опухолей относятся:
- В пищеводе Нарастающие жалобы при глотании по мере увеличения размеров опухоли, в результате чего возникают проблемы с приемом пищи.
- При опухоли ГИСО в желудке или двенадцатиперстной кишке Тошнота (часто, но не всегда), боли желудка или чувство быстрого насыщения желудка.
- В тонком кишечнике Запоры, «черный» стул (признак возможных кровотечений в кишечнике, вызванных опухолевыми процессами).
- Во всех случаях Потеря веса из-за нарушения метаболических процессов в организме. Анемия из-за скрытого кровотечения, вызванного опухолью, и поступления недостаточного количества питательных веществ, в результате чего развивается сильная слабость и общее истощение организма.
Симптоматика стромальных опухолей
Симптоматика ГИСО схожа с другими опухолями органов ЖКТ и может включать в себя:
- Скрытые кровотечения;
- Желудочно-кишечные кровотечения;
- Кишечная непроходимость;
- Увеличение живота;
- Ощущение быстрого насыщения;
- Боли;
- Слабость.
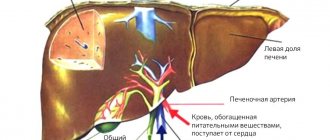
Особо стоит отметить, что у больных нередко (от 10 до 25% случаев, в зависимости от типа новообразования), наблюдается метастазирование стромальных опухолей в печень, брюшину, региональные лимфоузлы, легкие, мягкие ткани, редко в головной мозг.
получить бесплатную консультацию
Диагностика и определение стадии опухоли
При принятии решения по тактике и методу лечения важным элементом является тщательная диагностика рака, направленная на установление точного диагноза и определение степени распространения заболевания в организме. Подробная информация по диагностике ГИСО представлена в таблице ниже:
| Обследования | Примечания |
| Физикальный осмотр | |
| Анализ крови | Для оценки функции органов (общий анализ крови, почечные и печеночные показатели, свертываемость, ТТГ) |
| Эндоскопия, эндосонография | Для определения рисунка распространения заболевания, а также для получения биоматериала для гистологического подтверждения диагноза |
| КТ грудной клетки, живота, таза (с контрастом) |
|
| ПЕТ-КТ | (в отдельных случаях) Для подтверждения диагноза и определения стадии заболевания |
| Гистология |
|
| Молекулярная генетика | Мутации гена KIT/PDGFR при первичном диагнозе, в динамике при резистентности заболевания к терапии |
Преимущества лечения в Бельгии
- Доступность новейших препаратов. В Бельгии при резистентности опухоли к терапии иматинибом, сунитинибом и регорафенибом у больного есть возможность получить лечение новыми препаратами — сорафенибом, дасатинибом и нилатанибом. Это помогает продлевать жизнь даже в самых сложных случаях.
- Лапароскопическая малоинвазивная хирургия. Она используется в Бельгии при новообразованиях, не превышающих 5 см, расположенных в желудке и тонкой кишке. Преимущества лапароскопической резекции включают более быстрое возобновление нормального питания, более короткое пребывание в стационаре после операции и меньшее использование анальгезии. Краткосрочные результаты при этом остаются такими же, как и при открытой операции.
- Стоимость лечения. Она в Бельгии примерно на 30% ниже, чем в соседних странах Европы и на 60% ниже, чем в США. С учетом высокой стоимости лекарств, этот факт приобретает особую важность.
Прогностические факторы
Самыми важными клиническими прогностическими факторами являются митотический индекс, размер опухоли и локализация первичной опухоли. Для оценки вероятности возникновения метастазов проводится различие между возможными категориями риска, которые обобщены в таблице ниже:
| Риск прогрессии / рецидива заболевания | |||||||||
| Количество митозов | Размер (см) | Желудок | % | 12-перстная кишка | % | Тонкий кишечник | % | Прямой кишечник | % |
| ≤ 5 на 50 HPF | ≤ 2 | риска нет | 0 | риска нет | 0 | риска нет | 0 | риска нет | 0 |
| >2 ≤ 5 | очень низкий | 1,9 | низкий | 8,3 | низкий | 4,3 | низкий | 8,5 | |
| >5≤ 10 | низкий | 3,6 | высокий | 34 | средний | 24 | высокий | 57 | |
| > 10 | средний | 12 | высокий | 52 | высокий | 52 | |||
| > 5 на 50 HPF | ≤ 2 | риска нет | 0 | инфо отсутствует | — | высокий | 50 | высокий | 54 |
| >2 ≤ 5 | средний | 16 | высокий | 50 | высокий | 73 | высокий | 52 | |
| >5≤ 10 | высокий | 55 | высокий | 86 | высокий | 85 | высокий | 71 | |
| > 10 | высокий | 86 | высокий | высокий | 90 | высокий | |||
Симптомы
До 75% ГИСО обнаруживаются, когда они меньше 4 см в диаметре и либо бессимптомны, либо связаны с неспецифическими симптомами. Их часто диагностируют случайно во время рентгенологических исследований или эндоскопических или хирургических процедур, выполняемых для исследования заболевания желудочно-кишечного тракта или для лечения неотложных состояний. В Японии массовый скрининг на аденокарциному желудка с помощью верхней эндоскопии привел к увеличению случайных выявлений бессимптомных ГИСО.
В популяционном исследовании средний размер опухолей ГИСО, которые были обнаружены как случайные находки, составлял 2,7 см, по сравнению с 8,9 см для тех, которые были обнаружены на основании симптомов.
Верхнее кровотечение из желудочно-кишечного тракта — наиболее распространенное клиническое проявление ГИСО. Оно отмечается у 40-65% пациентов. Пациенты, которые испытали значительную потерю крови, могут сообщать о недомогании, усталости или одышке при физической нагрузке.
Обструкция может возникать в результате внутрипросветного роста эндофитной опухоли или из-за компрессии просвета из-за экзофитного поражения. Обструктивные симптомы могут быть органоспецифическими (например, затруднение глотания при опухоли пищевода, запор при ректальной опухоли, механическая желтуха при опухоли двенадцатиперстной кишки).
Другие симптомы:
- боль в животе;
- анорексия;
- тошнота;
- рвота;
- потеря веса;
- давление в эпигастрии;
- быстрая насыщаемость.
Методы терапия ГИСО
Оптимальная стратегия лечения рака в Германии при диагностированных гастроинтестинальных стромальных опухолях преследует две цели: местно-регионарный контроль за опухолью и профилактика/лечение отдаленных метастазов. Стратегия также зависит от стадии опухоли, прогностических факторов (гистология, митотический индекс, размер и локализация опухоли), а также от специфических для каждого отдельного пациента факторов. Приблизительный алгоритм действий представлен в схеме 1 ниже.
Активное наблюдение
Лечение маленьких гастроинтестинальных стромальных опухолей желудка (<2 см) ассоциируется — после резекции опухоли — с очень небольшой вероятностью возникновения рецидива, в связи с чем в отдельных случаях (например, возраст, коморбидность, периоперационные риски) можно рассмотреть вариант регулярного контроля и наблюдения за течением болезни (стратегия watch-and-wait). При этом важными являются условия, что опухоль не превышает 2 см, и при эндоскопическом/эндосонографическом контроле (каждые 3-6 месяцев) не наблюдается значительного роста ГИСО. Маленькие новообразования с другой локализацией (особенно в прямом кишечнике) склонны часто к рецидивам (к появлению метастазов), в связи с чем они, как правило, первично должны быть удалены хирургическим путем.
Хирургическое лечение
В зависимости от состояния опухоли и особенностей ее развития, выбирается один из вариантов операционного вмешательства.
- Хирургическое лечение первичной опухоли В случае, если первичная ГИСО изначально кажется резектабельной, показана первичная резекция опухоли. Как правило, при желудочной опухоли данное вмешательство проводится путем клиновидной резекции (англ. wedge resection), насколько возможно в пределах 1-2 см здоровых тканей. В случае необходимости может быть показана сегментарная резекция (тонкого или толстого кишечника) или en-bloc резекция (сальника). Как правило, лимфаденэктомия не показана, т. к. гастроинтестинальные стромальные опухоли редко метастазируют в лимфатические узлы. В случае же если R0-резекция не представляется возможной или необходима очень обширная операция, то сначала показана предоперационная (неоадъювантная) терапия препаратом Imatinib.
- Хирургическое лечение метастазов Данные проспективных исследований по резекции метастазов отсутствуют. Некоторые, но не все, ретроспективные исследования показали более благоприятный прогноз у пациентов, которым была проведена вторичная резекция, в основном после неоадъювантной терапии Imatinib и при хорошем ответе на проводимое лечение. В том случае, если возможна полная резекция опухоли/метастазов, то ее следует проводить в период хорошей реакции болезни на проводимую терапию (частичная ремиссия или стабильное заболевание). Однако даже при минимальном прогрессировании заболевания во время медикаментозной терапии прогноз течения заболевания значительно ухудшается, а при общем прогрессировании заболевания операция не показана из-за неблагоприятных прогнозов. Следует отметить, что медикаментозная терапия должна быть обязательно продолжена даже при полном удалении метастазов/опухоли.
- Вторичная резекция ГИСО и ее метастазов после индукционной терапии Imatinib На сегодняшний момент рандомизированные проспективные исследования не показали, что резекция остаточных манифестаций опухоли после индукционной терапии Imatinib создает лучшие прогнозы течения заболевания у пациентов. Однако, ретроспективные исследования указывают на то, что вторичная резекция связана с лучшими прогнозами течения болезни в том случае, если данное хирургическое лечение в Германии проводится у пациентов, которые хорошо отвечают на терапию (регресс опухоли или стабильное заболевание), в некоторых случаях даже при фокальном прогрессировании опухоли, а также при условии, что может быть проведена R0-резекция опухоли/метастазов. При мультифокальном прогрессировании и/или заранее прогнозируемой R2-резекции элективная резекция опухоли/метастазов не показана.
Лучевая терапия
Возможными паллиативными показаниями к лучевой терапии может являться лечение редко возникающих метастазов в костях или резектабельных ГИСО неблагоприятной локализации (например, в прямом кишечнике или в пищеводе), когда заболевание не реагирует на медикаментозную терапию.
Медикаментозная терапия
В зависимости от особенностей опухоли и ее реакции на осуществляемое лечение, подбирается наиболее эффективный вариант медикаментозной терапии.
- Неоадъювантная терапия (Imatinib) В случае, если полная резекция первичной опухоли не представляется возможной из-за ее размера и/или локализации, то сначала показана предоперационная (неоадъювантная) терапия медикаментом Imatinib для уменьшения размера опухоли. Следует отметить, для определения прогностического фактора ответа болезни на предстоящее лечение Imatinib, важно определить генотип KIT/PDGFRA, в связи с чем клетки ГИСО исследуются на отсутствие/наличие мутации генов. При мутации PDGFRA-D842V, которая делает опухоль резистентной к Imatinib, неоадъювантная терапия не показана, та же тенденция присутствует и при опухолях KIT-Wildtyp. Во время терапии Imatinib текущий контроль проводится каждые 3-4 месяца. По достижению ремиссии показана резекция опухоли (подробная информация см. выше), как правило, в течение 6-12 месяцев.
- Адъювантная терапия (Imatinib) Адъювантная (послеоперационная) терапия показана пациентам с значительным риском рецидива (см. таблицу выше), в то время как пациентам, относящимся к группе с низким риском возникновения рецидива, послеоперационная медикаментозная терапия не показана. Исследования показали, что терапия Imatinib в течение 36 месяцев (в сравнении с 12 месяцами) значительно улучшает период жизни без рецидива, хотя вопрос о точной длительности адъювантной терапии все еще является темой для дальнейших научных исследований и решение принимается в случае каждого отдельного пациента. Исследование генных KIT-/PDGFRA-мутаций является важным элементом в принятии решения по адъювантной терапии. С одной стороны, определение мутаций является прогностическим фактором, а с другой стороны не все мутации равнозначно/одинаково отвечают на терапию Imatinib, именно по этой причине необходимо провести тщательный анализ клеток опухоли на наличие/отсутствие мутаций.
- Аддитивная терапия Imatinib после метастазэктомии После метастазэктомии у большинства пациентов при отсутствии медикаментозной терапии в течение нескольких месяцев происходит прогрессирование заболевания, в связи с чем пациентам после метастазэктомии показана терапия Imatinib. Это также касается пациентов, которые получали предоперационную терапию Imatinib и у которых не было прогрессирования ГИСО. На данный момент не существует оптимальной продолжительности такого лечения, но, как правило, терапия Imatinib продолжается до тех пор, пока не будет выявлен рецидив болезни.
- Метастазированная гастроинтестинальная стромальная опухоль При метастазированной ГИСО медикаментозная терапия является терапией первого выбора. Подробный алгоритм медикаментозного лечения представлен в схеме 2 ниже.
Причины возникновения и факторы риска
Ученые обнаружили, что клетки могут расти неконтролируемым образом в результате нарушения в их ДНК. В ГИСО специфическая мутация заставляет клеточный фермент, известный как KIT, постоянно включаться.
KIT — это фермент (из группы внутриклеточных тирозинкиназ), ответственный за передачу сигналов роста и выживания внутри клетки. Если он включен, клетка растет или размножается. Выключение этого фермента переводит клетку в состояние покоя. Гиперактивный, неконтролируемый мутантный фермент KIT запускает быстрый рост и бесконечное размножение опухолевых клеток ГИСО.
Понимание этого процесса, уже помогло определить новые методы лечения этой неоплазии.
Факторы риска для ГИСО
Нейрофиброматоз
Наиболее существенным фактором риска для ГИСО становится наличие нейрофиброматоза. Он почти всегда связан с развитием таких новообразований.
Семейный анамнез
Есть редкие случаи появления наследственных ГИСО. Наследственные опухоли характеризуются унаследованными мутациями зародышевой линии в KIT или PDGFRA и дополнительными синдромами, такими как:
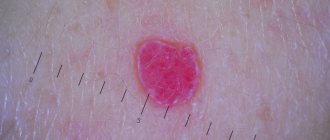
- кожная гиперпигментация;
- синдром раздраженного кишечника;
- дисфагия;
- дивертикулез кишечника.
95% ГИСО — KIT-положительные. Но 5% не демонстрируют определяемой экспрессии KIT. В части этих KIT-негативных ГИСО мутации происходят в гене PDGFRA, а не в KIT. Было показано, что иммуноокрашивание с помощью PDGFRA помогает различать KIT-негативные ГИСО и другие желудочно-кишечные поражения мезенхимы.
Мутации BRAF и протеинкиназа Сθ (PKCtheta) также были зарегистрированы в небольшом количестве ГИСО без KIT/PDGFRA. Первоначальные исследования показывают, что ГИСО с мутацией BRAF имеют склонность к тонкой кишке и не связаны с высоким риском злокачественности.
Текущий контроль
После полной резекции опухоли текущий клинический контроль, включающий КТ брюшной полости/таза, а также часто КТ грудной клетки (в зависимости от агрессивности опухоли) следует проводить каждые 3-6 месяцев в течение первых 5 лет, а затем один раз в год. Для небольших опухолей (<2 см) при необходимости можно выбрать более длительные интервалы. Следует отметить, что при длительном периоде ремиссии и при низком риске рецидива в качестве контроля можно также проводить МРТ брюшной полости для снижения уровня облучения организма. Ультразвуковое исследование в качестве текущего контроля не рекомендовано из-за его неспособности отображать перитонеальные метастазы. Гастроскопия как последующий вид контроля в настоящее время больше не рекомендована, так как частота локального рецидива после полной резекции опухоли очень низкая.
В качестве контроля при метастазированной ГИСО рекомендована КТ брюшной полости и таза (для обнаружения перитонеальных и печеночных метастазов) каждые 3-4 месяца. Как правило, рекомендуется также КТ грудной клетки для исключения или выявления пульмональных метастазов.
Где лечат ГИСО в Германии
Лечение русскоговорящих пациентов с гастроинтестинальными стромальными опухолями осуществляется по клиническим рекомендациями онкологов клиники «Нордвест». Больница оборудована высокотехнологичным оборудованием, позволяющим быстро и точно собрать данные для постановки диагноза. С момента обращения, весь период лечения и до момента выписки каждого пациента сопровождают прямые представители клиники, менеджеры-переводчики. Наши сотрудники помогут оформить необходимые документы, решить попутно возникающие вопросы. Перед поступлением в больницу Nordwest вы можете предварительно обсудить свой диагноз с доктором с помощью видеоконсультации.