Симптомы Классификация Диагностика Лечение Информационный блок
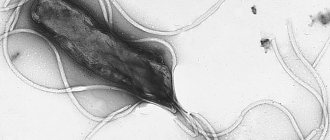
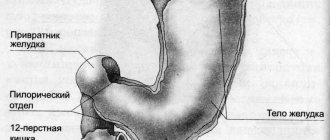
Хронический гастрит — воспаление слизистой оболочки желудка, возникающее под воздействием факторов различной этиологии (бактериальных, химических, термических и механических).
ИНСТИТУТ АЛЛЕРГОЛОГИИ И КЛИНИЧЕСКОЙ ИММУНОЛОГИИ располагает:
- спектром услуг для точной диагностики заболеваний
- специальными программами лечения
- консультации
- проводят врачи, имеющие ученые степени.
При выявлении сопутствующих заболеваний проводятся консультации со специалистами смежных областей (оториноларингологи, эндокринологи, неврологи, гастроэнтерологи, дерматовенерологи), консилиумы с Докторами медицинских наук.
Внимание! Одни и те же симптомы могут быть признаками разных заболеваний! Не занимайтесь самолечением, обратитесь к врач-гастроэнтерологу!
Симптомы
| При повышенной кислотности | При пониженной кислотности |
| Изжога Отрыжка кислым Тупая ноющая боль в эпигастрии после приема пищи Ощущение тяжести, давления в эпигастрии после приема пищи Запоры Понижение аппетита | Отрыжка воздухом Тошнота, рвота Жгучие боли после приема пищи в эпигастрии Диарея Метеоризм, урчание в животе. |
Классификация
Сиднейская система классификации хронических гастритов
| Тип гастрита | Синонимы (прежние классификации) |
| Неатрофический | Поверхностный Хронический антральный Гастрит типа В Гиперсекреторный гастрит |
| Атрофический аутоиммунный | Гастрит типа А Диффузный гастрит тела желудка, ассоциированный с В12-дефицитной анемией и с пониженной секрецией |
| Атрофический мультифокальный | Смешанный гастрит типа А и В |
| Химический | Реактивный гастрит типа С Реактивный рефлюкс-гастрит |
| Радиационный | |
| Лимфоцитарный | Гастрит, ассоциированный с целиакией |
| Гранулематозный | Изолированный гранулематоз |
| Эозинофильный | Аллергический |
| Другие инфекционные | Бактерии (кроме Helicobacter pylori) Грибы, Паразиты |
| Гигантский гипертрофический | Болезнь Менетрие |
По клинической картине
| хронический гастрит типа А | гастрит типа В | тип С |
| первичный аутоимунный гастрит дна желудка (фундальный) | антральный гастрит бактериального происхождения | рефлюкс-гастрит |
| По происхождению | По состоянию секреторной функции | По гистологической картине | По анатомическому расположению зоны воспаления |
| бактериальный, аутоиммунный, эндогенный, ятрогенный, рефлюкс-гастрит | пониженная повышенная нормальная | поверхностный, атрофический, гиперпластический | антральный фундальный |
Волгоград
По ЧАСТОТЕ:
Тип — А: 5%,
тип — В: 85%,
тип — С: 10% всех пациентов с хроническим гастритом
В возрасте >50 лет 50% людей имеют хронический поверхностный гастрит типа В.
2 классификационные системы гастрита:
АВС-классификация хронического гастрита:
В её основе: этиологические и гистологические критерии.
Тип А (синонимы — гастрит тела желудка, аутоимунный гастрит).
Особенности: нисходящее распространение от слизистой кардии до тела желудка.
Суть патогенеза: это аутоимунное заболевание с аутоантителами на обкладочные (париетальные) клетки в 90%, а также с аутоантителами на внутренний фактор Касла в 70%.
В результате исчезновения обкладочных клеток развивается ахлоргидрия (т.е. отсутствие НСL).
А из-за недостатка внутреннего фактора Касла может возникнуть В12-дефицитная анемия (или т.н. пернициозная анемия).
У пациентов с хроническим гастритом тела желудка могут быть также другие аутоимунные заболевания, такие как:
- болезнь Аддисона,
- тиреоидит Хашимото.
Тип В (синонимы — гастрит антрального отдела, HP-gastritis вызванный Helicobacter pylori)
Плотность населения геликобактерий определяет:
- степень гастрита, которая зависит от инфильтрации слизистой лимфоцитами и плазмоцитами,
- и активность гастрита, которая зависит от инфильтрации слизистой нейтрофильными гранулоцитами.
Особенности: гастрит типа В имеет восходящее распространение, в результате чего граница antrum/corpus перемещается вверх, наступает уменьшение количества обкладочных клеток и развивается гипохлоргидрия, НО!!! На фоне гипохлоргидрии никогда не наступает ахлоргидрия.
В основе патогенеза: инфицирование слизистой желудка Helicobacter Pylori: грам-отрицательные бактерии с высокой активностью уреазы, что создаёт возможность быстрого подтверждения при помощи экспресс-методов.
Тип С (синонимы — химически индуцированный гастрит):
В основе лежит гастрит, вызванный желчным рефлюксом, который может развиться, например, в культе желудка после операции Бильрот-I или Бильрот-II.
Редкие особые формы гастрита, например:
Гастрит Крона: желудочные проявления болезни Крона: непрерывная инфильтрация слизистой желудка гранулоцитами + подтверждение эпителиально-клеточной гранулёмы. Поэтому даже при подозрении на эту патологию необходима диагностика нижнего пищеварительного тракта на предмет болезни Крона, обязательная отсроченная ФКС.
Классификация гастрита по Sidney (1990 г.):
В её основе: этиологические, гистологические и эндоскопические критерии.
Этиология: как при АВС — классификации гастритов.
Топографически:
- гастрит антрального отдела,
- гастрит тела,
- пангастрит
A. Эндоскопические категории гастрита:
- Эритематозный (эксудативный) гастрит,
- Гастрит с плоскими эрозиями,
- Гастрит с полипоидными эрозиями,
- Атрофический гастрит (складки слизистой сглажены или полностью исчезли),
- Геморрагический гастрит,
- Рефлюкс-гастрит (рефлюкс желчи в желудок),
- Гастрит с гигантскими складками.
B. Гистологические параметры гастрита:
морфология включает в себя 5 параметров:
I. Хронический гастрит: показатели:
- инфильтрация lamina propria лимфоцитами и плазмоцитами (которые в нормальной слизистой желудка не обнаруживаются),
- образование лимфатические фолликулов
- по размеру лимфоплазмоклеточной инфильтрации различают 3 степени тяжести.
II. Активность воспалительного процесса: кореллирует с плотностью нейтрофильных гранулоцитов, при этом различают 3 степени активности.
III. Атрофия тела желудка: редукция специфических желез желудка, к ним относятся, главные и обкладочные клетки. Атрофический гастрит в области дна и тела желудка типичен для аутоиммунного гастрита.
IV. Кишечная или интестинальная метаплазия подразделяют 3 типа:
Тип I: полная интестинальная метаплазия, преобразование по типу слизистой тонкого кишечника,
Тип II: неполная интестинальная метаплазия с подтверждением наличия бокаловидных клеток.
Тип III: неполная метаплазия колического или энтероколического типа
V. Заселение Helicobacter pylori (HP).
Модифицированная Сиднейская Система классификации ХГ.
| Тип гастрита | Синонимы | Этиологические факторы |
| Неатрофический | Поверхностный, диффузный антральный хронический антральный, интерстициальный, | тип В H.pylori, другие факторы |
| Атрофический: Аутоиммунный Мультифокальный | Тип А, диффузный тела желудка, ассоциированный с пернициозной анемией | Аутоиммунный H.pylori, особенности питания, факторысреды |
| Особые формы: Химический Радиационный Лимфоцитарный Неинфекционный гранулематозный Эозинофильный Другие инфекционные | Реактивный рефлюкс-гастрит, тип С Вариломорфный, ассоциированный с целиакией Изолированный гранулематоз Пищевая аллергия, другие аллергены | Химические раздражи-тели, желчь, НПВП Лучевые поражения Идиопатический, иммунные механизмы, глютен, H.pylori Болезнь Крона, саркои-доз, гранулематоз Вегенера, инородные тела, идиопатический Аллергический Бактерии (кроме H.pylori), вирусы, грибы, паразиты |
ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ:
Уровень сывороточного гастрина при гастрите тела желудка высокий или очень высокий в зависимости от снижения продукции HCL.
При антрум гастрите (место секреции гастрина) уровень гастрина наоборот сравнительно низкий.
ОСЛОЖНЕНИЯ:
- Рецидивирующая язвенная болезнь на основе геликобактерного гастрита.
- Пернициозная анемия — иначе В12-дефицитная анемия при гастрите типа А.
- Повышенная частота карциномы желудка при атрофическом гастрите типа. А и при НР-гастрите с интестинальной метаплазией.
- Повышенный риск развития первичной лимфомы желудка типа MALT при геликобактерном гастрите.
МАLТ — Mucosa associated lymphoid tissue — мукозо-ассоциированная лимфоидная ткань
ДИАГНОЗ:
- Гастроскопия с биопсией из антрального отдела и корпуса желудка + обследование на геликобактерии.
- Диагностика Helicobacter pyiori(HP): Эндоскопически-биопсическая: быстрый тест на уреазу, гистология, цитология, высев культуры,
- 13C — или 14С — дыхательный тест: после введения радиактивно меченной мочевины, образующей под воздействием геликобактерии собственную уреазу, во выдыхаемом воздухе измеряется меченый С02.
- Серологическая (подтверждение антител). После успешного лечения, титр антител в течение полу-года уменьшается приблизительно на 50% от исходного уровня.
- Разграничивающая диагностика при гастрите типа А: Аутоантитела против париетальных клеток, Аутоантитела против внутреннего фактора Касла,
- уровень витамина B12 в сыворотке.
ВНИМАНИЕ!!! Диагноз хронического гастрита можно выставить и диагностировать только эндоскопически с гистологическим анализом.
Это же относится к диагностике HP.
Причины
| Тип гастрита | Этиологические факторы |
| Неатрофический | Helicobacter pylori Другие факторы |
| Атрофический аутоиммунный | Иммунные механизмы |
| Атрофический мультифокальный | Helicobacter pylori Нарушения питания Факторы среды |
| Особые формы | |
| Химический | Химические раздражители: желчь (ДГР) приём НПВП |
| Радиационный | Лучевое поражение |
| Лимфоцитарный | Идиопатический Иммунные механизмы Глютен |
| Гранулематозный | Болезнь Крона Саркоидоз ГранулематозВегенера Инородные тела Идиопатический |
| Эозинофильный | Пищевая аллергия Другие аллергены |
| Другие инфекционные заболевания | Бактерии (кроме Helicobacter pylori) Грибы, Паразиты |
| Гигантский гипертрофический | Болезнь Менетрие |
| Экзогенные (внешние) | Эндогенные (внутренние) |
| 1.Нарушение режима питания: большие промежутки между едой, поздние и ночные ужины, питание в сухомятку, глотание плохо пережеванной пищи. 2.Прием продуктов, раздражающих слизистую желудка: острое, копченое, кислое, соленое, грубая пища, крепкий кофе, алкоголь, обжигающе горячая или холодная пища, употребление недоброкачественных продуктов. 3. Химические вещества и лекарственные препараты. 4. Курение. 5. Психологически тяжелые, стрессовые состояния. 6. Вредное производство (большая задымленность или запыленность атмосферы на рабочем месте). | 1.Helicobacter pylori (HP) 2.Паразитарные инфекции 3.Тяжелые инфекционные заболевания (туберкулез и др.). 4.Эндокринные патологии (сахарный диабет, патологии щитовидной железы). 5.Нарушения иммунитета. 6.Нарушенное дыхание или патологии кровеносной системы. 7.Дуоденогастральный рефлюкс. |
Университет
→ Главная → Университет → Университет в СМИ → Варианты течения хронического гастрита
Фото носит иллюстративный характер. Из архива «МВ»
Иван Броновец, профессор кафедры кардиологии и внутренних болезней БГМУ, доктор мед. наук
Хронический гастрит (ХГ) — рецидивирующее очаговое или диффузное воспаление слизистой и подслизистой оболочки желудка, сопровождающееся нарушением регенерации, со склонностью к прогрессированию, развитию атрофии и секреторной недостаточности. Основные изменения возникают в слизистой оболочке, поэтому изучается функциональная морфология слизистой, а не всего желудка.
Хронический гастрит занимает ведущее место среди болезней органов пищеварительной системы. Различные варианты патологии диагностируют у 50–75 % пациентов старше 45 лет.
Классификация
Всеобщее признание получила Сиднейская классификация гастрита (1990), модифицированная в Хьюстоне (1994). Она объединяет этиологический, топографический и морфологический принципы оценки заболевания. По этиологии ХГ делят на хеликобактерный (тип В), аутоиммунный (тип А), химический, или рефлюксный, гастрит (тип С) и особые формы (лимфоцитарный, радиоцитарный, гранулематозный, эозинофильный гастрит и др.).
Топографически различают гастрит тела желудка, антрального, фундального и/или всех отделов желудка (пангастрит). По морфологическим признакам оценивают наличие и степень воспаления, атрофии, метаплазии, обсеменение бактериями хеликобактер пилори (Helicobacter pylori, HP). Гастрит делят на эрозивный и неэрозивный. ХГ может быть поверхностным и глубоким (трансмуральным).
Кроме основных этиологических факторов в развитии и прогрессировании ХГ играют роль нарушение режима питания, грубая пища, злоупотребление специями, алкоголем, курение, систематическая травматизация слизистой оболочки желудка плохо измельченной пищей, торопливая еда и др.
Хеликобактерный ХГ в основном поражает антральный отдел желудка. HP наиболее часто выявляется на покровном эпителии под слоем слизи (поверхностный гастрит) и значительно реже при атрофическом гастрите.
Главная морфологическая особенность этого вида гастрита — наличие на слизистой оболочке НР в бициллярной форме и в виде кокков. Поражаются поверхностный эпителий, появляется лейкоцитарная инфильтрация. Важное значение в диагностике имеет определение НР и степень обсеменения антрального отдела. Золотым стандартом диагностики считается исследование биоптатов не только из антрального отдела, но и из области тела желудка.
Аутоиммунный ХГ встречается значительно реже, чем НР-ассоциированный. Диагностируют у 16 % больных с макроцитарной гиперхромной (пернициозной) анемией. Характерной особенностью является локализация изменений в фундальном отделе желудка, в то время как антральный отдел остается непораженным.
Это приводит к резкому снижению кислотности и внутреннего фактора. Дефицит внутреннего фактора служит причиной мальабсорбции витамина В12 и развития пернициозной анемии. Развивается тяжелый атрофический гастрит с прогрессирующей потерей массы париетальных клеток.
Протекает бессистемно, пока не разовьется одно из осложнений (дефицит витамина В12 или злокачественное поражение желудка); появляется метаплазия. На конечной стадии отмечается полное метапластическое замещение слизистой оболочки. Выявляются титры антител к париетальным клеткам и внутреннему фактору, ахлоргидрия.
Рефлюкс-гастрит связан с забросом содержимого двенадцатиперстной кишки в желудок, повреждающего его слизистую оболочку. Истинный рефлюкс-гастрит развивается у пациентов, перенесших резекцию желудка.
Синоним рефлюкс-гастрита — щелочной гастрит. Он не вполне точен, так как основную роль в повреждении слизистой оболочки желудка играют не щелочные свойства кишечного содержимого, а особенности желчных кислот. К тому же необходимым условием развития гастрита является наличие соляной кислоты.
Главная составляющая дуоденального содержимого — желчные кислоты, их соли, панкреатические ферменты и лизолецитин. Желчные кислоты вызывают повреждение защитного барьера желудочной слизи, способствуя повышению обратной диффузии ионов водорода, а при низкой желудочной секреции ферменты поджелудочной железы могут также повреждать слизистую оболочку желудка.
При ХГ, особенно прогрессирующем, часто встречается метаплазия слизистой оболочки желудка по кишечному типу. Речь идет о замещении желудочного эпителия кишечным. При атрофическом гастрите и раке желудка метаплазия наблюдается почти в 100 % случаев. В настоящее время принято выделять два типа метаплазии: полную, напоминающую тонкую кишку, и неполную (толстую). Наличие клеток Панета — наиболее важный признак полной кишечной метаплазии.
Диагностика
Для постановки клинического диагноза необходимо правильно диагностировать тип ХГ, оценить степень и распространенность атрофии и других морфологических признаков заболевания. Дисрегенерация определяет морфогенез и клинико-морфологическую картину ХГ.
О наличии хронического воспаления можно вести речь лишь тогда, когда оно обнаружено при морфологическом исследовании. До биопсии клиницист вправе диагностировать ХГ и может применять лишь синдромологическое обозначение «неязвенная диспепсия».
Эндоскопический метод исследования позволяет с большой точностью определять диагноз (либо существенно уменьшать число предлагаемых диагнозов), осматривать все отделы желудка, брать биоптаты для гистологического исследования.
Возможности эндоскопического исследования не ограничиваются только визуальным осмотром полости желудка и взятием биоптатов, существует целый ряд дополнительных методик, использующихся вместе с эндоскопией (хромогастроскопия, трансэндоскопическая рН-метрия). Гастроскопия с полным клинико-морфологическим исследованием биоптатов слизистой оболочки желудка (с определением Hp) считается корректным методом диагностики различных вариантов поражения желудка.
Самая частая причина (70–80 %) хронического гастрита — бактерия хеликобактер пилори. Аутоиммунный гастрит диагностируется в 15–18 % случаев, около 10 % приходится на НПВС, менее 5 % составляет рефлюкс-гастрит, 1 % — редкие формы ХГ.
Фото: Евгений КречМедицинский вестник, 5 октября 2017
Поделитесь
Диагностика
Уреазный дыхательный тест — самый инновационный и точный анализ на Helicobacter pylori! Лучший метод контроля качества лечения!
ИНСТИТУТ АЛЛЕРГОЛОГИИ И КЛИНИЧЕСКОЙ ИММУНОЛОГИИ располагает фундаментальной базой, позволяющей провести весь комплекс диагностических и лечебных мероприятий, соответствующих уровню международных стандартов. Многие из лечебно-диагностических методов разработаны сотрудниками нашего Института.
Диагноз устанавливается на основании клинической картины и анамнеза пациента, физикального исследования, лабораторной диагностики, эндоскопии (гастроскопия), проведение биопсии и др. исследований.
При необходимости консультативную помощь Вам могут оказать смежные специалисты, опытные врачи, разрабатывающие новые методы диагностики и лечения в этих направлениях медицины.
Каждый пациент с хроническим гастритом должен помнить, что гастрит-причина развития других патологий желудочно-кишечного тракта!
Лабораторная диагностика направлена на выявление причины хронического гастрита, определение уровня гастрина, пепсиногена (соотношение пепсиногена I и пепсиногена II) в крови, содержание витамина В12 в сыворотке. Может проводиться бактериологическое исследование, биохимическое обследование и др. исследования.
Хронический гастрит: современные представления, принципы диагностики и лечения
Ивашкин В.Т., Лапина Т.Л.
«Хронический гастрит» или «хронический гастродуоденит» — диагноз, который чрезвычайно часто реализуется в медицинской практике, причем не всегда его формулировка отражает существенную сторону заболевания у конкретного больного. Можно сказать, что это «дежурный» диагноз для больного, который обратился к врачу по поводу диспептических жалоб и у которого при эндоскопии не обнаружена язва. За последние годы медицинской наукой был сделан значительный шаг вперед, позволивший на качественно новом уровне знаний пересмотреть наши представления о гастрите.
Решающее значение имело открытие нового вида микроорганизма — бактерии Helicobacter pylori (H.pylori) — и изучение ее роли в патологии человека. Стало очевидным, что этот микроб, колонизирующий слизистую оболочку желудка, выступает возбудителем наиболее частого из вариантов гастрита. Действительно, именно установление этиологического значения H.pylori сделало хронический гастрит четко очерченной и клинически значимой нозологической единицей, превратило его из аморфного понятия в заболевание с известной причиной, прослеживаемыми этапами патогенетического развития, определенным прогнозом и, наконец, создало возможности этиотропного лечения. Классические представления о гастрите благодаря H.pylori приобрели большую устойчивость, так как это фрагмент знания позволил сбалансировать имевшуюся информацию о морфологических и функциональных изменениях (кислотная продукция, слизеобразование и др.) и связи гастрита с другими заболеваниями, в первую очередь, — язвенной болезнью и раком желудка [2,3,4].
Вторым существенным шагом стала разработка современной классификации гастритов. Так называемая Сиднейская система была предложена в 1990-м и дополнена в 1994 году. С тех пор, хотя и не лишенная недостатков (как любая классификация), Сиднейская система признана почти во всем мире. Она оказалась удобной в повседневной диагностической практике, обеспечила единый концептуальный подход и язык в описании изменений желудка. Безусловным положительным качеством классификации следует считать предложенную визуально-аналоговую шкалу для полуколичественного определения активности и выраженности гастрита, атрофии и кишечной метаплазии, степени колонизации H.pylori, что существенно снизило субъективность оценок при характеристике гистологической картины.
Хронический гастрит, вызванный инфекцией H.pylori
- Частота
Инфекция H.pylori имеет глобальное значение и широко распространена, в том числе и в нашей стране, где по эпидемиологическим данным инфицированы более 80% взрослого населения. H.pylori практически у всех инфицированных индивидуумов вызывает воспалительные изменения в гастродуоденальной слизистой оболочке, которые и представляют собой собственно субстрат гастрита. Геликобактерный гастрит — наиболее распространенный вариант гастрита. Так, около 5% всех больных гастритом страдают аутоиммунным гастритом, еще 5% — другими особыми формами гастрита, о которых речь пойдет ниже. Таким образом, воспаление слизистой оболочки желудка, вызванное H.pylori, составляет 90% среди всех форм гастритов.
- H.pylori — этиологический фактор хронического гастрита
После приема per os культуры H.pylori удалось воспроизвести возникновение типичных для гастрита морфологических изменений в ранее нормальной слизистой оболочке в опытах по самозаражению, один из которых провел первооткрыватель бактерии Б. Маршалл. Проводятся исследования на лабораторных животных, у которых воспроизводится формирование гастрита под воздействием бактерии-возбудителя.
Заражение H.pylori приводит к появлению воспалительного инфильтрата в слизистой оболочке желудка, а присутствие H.pylori всегда сопровождается морфологическими признаками гастрита. Инфильтрация полиморфноядерными лейкоцитами (нейтрофилами) непосредственно вызвана бактерией, которая выделяет особый белок, активирующий нейтрофилы. Ген, кодирующий его синтез (napA) выявлен у всех штаммов H.pylori. Таким образом, этому микроорганизму присуще специфическое качество вызывать нейтрофильную инфильтрацию слизистой оболочки желудка, характеризующую активность гастрита. Адгезия H.pylori к клеткам желудочного эпителия, так же как адгезия в случае любой другой бактериальной инфекции слизистой оболочки, вызывает реорганизацию цитоскелета эпителиоцитов и ряд других изменений; эпителиальные клетки отвечают на это продукцией цитокинов — интерлейкина-8 (IL-8) и некоторых других хемокинов. Эти цитокины также приводят к миграции лейкоцитов из кровеносных сосудов, развивается активная стадия воспаления. Активированные макрофаги секретируют интерферон-g и фактор некроза опухоли. Эти факторы сенситизируют рецепторы лимфоидных, эпителиальных и эндотелиальных клеток, что в свою очередь привлекает в слизистую оболочку новую волну клеток, участвующих в иммунных и воспалительных реакциях. Каталаза и супероксиддисмутаза, продуцируемые Н.pylori, нейтрализуют фагоциты, позволяют микробу избежать фагоцитоза и способствуют гибели полиморфноядерных лейкоцитов. Метаболиты активного кислорода нейтрофилов оказывают повреждающее действие на эпителиоциты желудка. Хроническая фаза инфекции отличается значительной лимфоцитарной инфильтрацией и потерей целостности эпителия.
Согласно современным представлениям, Н.pylori вызывает изменение нормальных процессов регенерации желудочного эпителия: микроорганизм обусловливает (прямо или косвенно) дисрегенераторные процессы, которые служат важной составляющей в патогенезе гастрита; Н.pylori влияет и на пролиферацию, и на апоптоз эпителиоцитов слизистой оболочки желудка. Понятно, что нарушение процессов клеточного обновления в слизистой оболочке желудка лежит в основе морфогенеза атрофии при гастрите.
Важное доказательство этиологической роли Н.pylori очень легко получить в повседневной практике, так как после успешного лечения инфекции наступает регрессия отдельных компонентов морфологической картины гастрита.
- Исходы инфекции H.pylori
Заражение H.pylori происходит преимущественно в детском возрасте и без лечения персистенция микроорганизма становится пожизненной. В зависимости от вирулентных свойств H.pylori и генетических особенностей макроорганизма исходы инфекции H.pylori различны: у большинства инфицированных хронический гастрит протекает бессимптомно, у части больных (по данным некоторых авторов, у 6% инфицированных) развивается язвенная болезнь, у части больных прогрессирование гастритических изменений приводит к развитию рака желудка. Несомненна связь H.pylori с редкой формой злокачественной опухоли желудка — лимфомой, исходящей из лимфоидной ткани, ассоциированной со слизистыми оболочками (MALT-лимфомы).
Исходы инфекции H.pylori зависят от варианта хронического гастрита, который, в свою очередь, во многом определяется топографией колонизации H.pylori гастродуоденальной слизистой оболочки. Дуоденальная язва возникает на фоне гастродуоденита, т.е. преимущественно антрального гастрита, а заселение слизистой оболочки двенадцатиперстной H.pylori возможно после формирования в ней очагов желудочной метаплазии в ответ на кислотную агрессию. Высказано предположение о том, что начальными центрами ульцерации при язвенной болезни двенадцатиперстной кишки оказыввются очаги метаплазии с адгезированными H.pylori и воспалительными изменениями. Язвы желудка формируются на фоне диффузного (пан-)гастрита или гастрита преимущественно тела желудка, при котором слизистая оболочка, «ослабленная» воспалением, подвергается воздействию факторов агрессии даже при нормальных показателях кислой секреции.
Инфекция H.pylori признана Международным Агентством по исследованию рака ВОЗ канцерогенной для человека. Связь H.pylori и рака желудка в настоящее время не вызывает сомнений, и связующим звеном рассматривается хронический гастрит. Длительная персистенция H.pylori сопровождает прогрессирование гастритических изменений: с годами гастрит становится атрофическим. Еще до открытия H.pylori было известно, что атрофический гастрит может рассматриваться, как предраковое заболевание. Значимость атрофического гастрита в канцерогенезе определяется частотой — на его долю приходится 3/4 в структуре предраковых заболеваний желудка. Известно, что риск развития карциномы желудка при атрофическом гастрите в 10 раз выше, чем в популяции. Дальнейшее углубление гастритического процесса связано с формированием кишечной метаплазии: особенно опасно появление неполной (или толстокишечной) метаплазии. Именно этот эпителий при определенных условиях может стать основой дисплазии и малигнизации. Таким образом, патогенетический каскад, запускаемый H.pylori и через стадии атрофии, метаплазии и дисплазии приводящий к раку желудка, хорошо изучен и приблизился к завершенности благодаря установлению этиологической роли бактерии для хронического гастрита.
Лечение хронического геликобактерного гастрита
Современная терапия хронического гастрита — это этиологическая терапия, направленная на эрадикацию инфекции H.pylori. Стандарты (протоколы) диагностики и лечения больных с заболеваниями органов пищеварения, утвержденные Министерством здравоохранения РФ, относят антигеликобактерные схемы к необходимым лечебным мероприятиям при гастрите с выявлением H.pylori. Однако мы знаем, что хронический гастрит, ассоциированный с H.pylori, — чрезвычайно широко распространенное заболевание. Имея основание для проведения антигеликобактерной терапии при гастрите, необходимо понять, каким конкретно больным показана эта терапия. Рекомендации по диагностике и лечению инфекции H.pylori, принятые для стран Европейского Союза в 1997 году (Маастрихтский консенсус — I) в качестве показания для эрадикационной терапии называли варианты гастрита с тяжелыми структурными изменениями — с кишечной метаплазией, атрофией, а также гастрит с эрозиями. В итоговом документе Второй согласительной конференции по диагностике и лечению инфекции H.pylori (Маастрихтский консенсус — II, 2000) в качестве безусловного показания к эрадикационной терапии установлена только одна форма гастрита — атрофический гастрит.
Анализ большого числа клинических испытаний позволяет выделить лучшие схемы для лечения инфекции H.pylori, отвечающие требованиям медицины, базирующейся на доказательствах. Эти схемы нашли отражение в итоговом документе Второй согласительной конференции по диагностике и лечению инфекции H.pylori (2000) В качестве начального курса лечения (терапия первой линии) предлагаются следующие схемы из трех препаратов как минимум на 7 дней: ингибитор протонной помпы (или ранитидин висмут цитрат) в стандартной дозе 2 раза в день + кларитромицин 500 мг 2 раза в день + амоксициллин 1000 мг 2 раза в день или метронидазол 500 мг 2 раза в день. Сочетание кларитромицина с амоксициллином предпочтительнее, чем кларитромицина с метронидзолом, так как может способствовать достижению лучшего результата при назначении лечения второй линии — квадротерапии.
В случае отсутствия успеха лечения начинается второй этап. Больному предлагается резервная схема (терапия второй линии — квадротерапия) как минимум на 7 дней: ингибитор протонной помпы в стандартной дозе 2 раза в день + висмута субсалицилат/субцитрат 120 мг 4 раза в день + метронидазол 500 мг 3 раза в день + тетрациклин 500 мг 4 раза в день.
В нашей стране в качестве терапии первой линии широко используются тройные схемы на основе препарата висмута (наиболее известен субцитрат коллоидного висмута). Следует отметить, что именно для лечения хронического гастрита такие схемы могут оказаться наиболее приемлемыми, так как при назначении эрадикации H.pylori в случае обострения язвенной болезни необходимость быстрого купирования болевого и диспептического синдрома заставляет отдать предпочтение схемам на основе ингибиторов протонной помпы. При хроническом гастрите, который не имеет симптоматики, тройные схемы на основе соли висмута могут оказаться оптимальными по соотношению «стоимость — эффективность».
Обратимость изменений, присущих хроническому гастриту, под влиянием эрадикации H.pylori
После эрадикации инфекции уже через месяц полностью исчезает нейтрофильная инфильтрация эпителия и собственной пластинки слизистой оболочки (отражающая активность гастрита), а в более поздние сроки исчезает мононуклеарная инфильтрация. Таким образом, хронический неатрофический гастрит полностью излечивается после уничтожения H.pylori. В отношении возможности обратного развития атрофии и кишечной метаплазии после эрадикации инфекции в литературе существуют противоречивые мнения. Возможно, что период наблюдения слишком ограничен для оценки таких изменений, однако были и исследования с относительно продолжительным катамнезом, которые также дали противоположные результаты. Тем не менее представляется вполне обоснованным, что успешная эрадикация H.pylori даже на этапе атрофии, приводит к прерыванию патологического каскада в слизистой оболочке желудка и может рассматриваться, как профилактика развития рака желудка. В пользу эрадикации H.pylori у больных атрофическим гастритом свидетельствует целый ряд работ (в том числе проведенных в нашей клинике), доказывающих, что уничтожение инфекции нормализует процессы клеточного обновления в слизистой оболочке желудка.
Хронический геликобактерный гастрит и функциональная диспепсия
Соотношение хронического геликобактерного гастрита и функциональной диспепсии
Диагноз гастрит — диагноз морфологический, то есть он может считаться правомочным после оценки гастробиоптатов специалистом — патологоанатомом. В соответствии с требованиями Сиднейской системы, для того чтобы правильно интерпретировать состояние слизистой оболочки желудка, необходимо минимум пять биоптатов: 2 — из антрального отдела на расстоянии 2-3 см от привратника по большой и малой кривизне, 2 — из тела желудка на расстоянии 8 см от кардии по большой и малой кривизне, 1 — из угла желудка.
«Клинический» диагноз гастрита, т.е. диагноз без морфологического исследования гастробиоптатов практически не имеет смысла. Жалобы, а это, как правило, симптомы диспепсии, которые заставляют больного обратиться к врачу, носят функциональный характер и не обусловлены теми морфологическими изменениями, которые составляют суть гастрита. Изменения, обнаруживаемые при эзофагогастродуоденоскопии (например, гиперемия слизистой оболочки), являются субъективными и лишь косвенным образом могут свидетельствовать о наличии гастрита, в особенности о степени его прогрессирования.
В случае жалоб на боли и дискомфорт в эпигастральной области и при отсутствии изъязвления при эндоскопии и для врача, и для пациента удобен синдромный диагноз функциональной диспепсии. Такой подход позволяет врачу применить весь возможный арсенал лекарственных средств и курортных факторов и установить доверительные отношения с больным, объясняя природу его недуга функциональными причинами.
Установлены критерии диагноза функциональной диспепсии (Римские критерии II). Врач вправе поставить этот диагноз при:
- наличии постоянной или повторяющейся диспепсии (боли и дискомфорт в эпигастральной области) по крайней мере в течение 12 недель (не обязятельно последовательных) в течение последних 12 месяцев;
- отсутствии органического заболевания (в том числе и по результатам эзофагогастродуоденоскопии), которое бы объясняло наличие перечисленных симптомов;
- отсутствии облегчения симптомов после дефекации и отсутствии их связи с изменением частоты и характера стула (то есть, исключен синдром раздраженной кишки).
В зависимости от преобладающего симптома выделяют варианты функциональной диспепсии: в том случае, если ведущим симптомом выступает боль в эпигастральной области, говорят о язвенноподобном варианте; если доминирующим симптомом служит дискомфорт — чувство переполнения в эпигастрии, раннее насыщение, вздутие живота, тошнота — о дискинетическом варианте; промежуточное состояние назвали неспецифическим вариантом.
Представления о патогенезе функциональной диспепсии все еще складываются. При установлении этого диагноза должны быть исключены органические заболевания — язвенная болезнь, гастроэзофагеальная рефлюксная болезнь, опухоли, заболевания панкреато-билиарной зоны и прием лекарств, например НПВП. Однако диагнозу функциональной диспепсии не противоречит наличие хронического гастрита, ассоциированного с инфекцией H.pylori. Значение присущих гастриту морфологических изменений для функциональной диспепсии практически не известно. По данным европейских авторов (для популяций с невысоким распространением H.pylori), инфекция H.pylori обнаруживается в 30-70% случаев функциональной диспепсии. Мета-анализ D. Armstrong (1996) продемонстрировал, что H.pylori чаще встречается у больных с диспепсией, чем в среднем в популяции.
Лечение функциональной диспепсии
Отсутствие полных представлений о патогенезе функциональной диспепсии, особенности больных (в том числе психологические) делают лечение этого синдрома непростой задачей.
Антацидные препараты (Алмагель) в повседневной практике применяются, как терапия первой линии при функциональной диспепсии. Антациды хорошо знакомы пациентам и врачам, известна безопасность их использования, поэтому эта группа препаратов всегда находит применение при функциональной диспепсии. Многие больные начинают прием антацидов еще до консультации врача и будут возвращаться к нему в дальнейшем, в том числе благодаря безрецептурному отпуску.
Блокаторы Н2-рецепторов гистамина — группа лекарственных препаратов, которую чаще всего применяют в лечении функциональной диспепсии. Результаты клинических исследований противоречивы. Некоторые авторы считают, что положительный результат от антагонистов Н2-рецепторов гистамина в ряде клинических испытаний получен благодаря группе больных с гастроэзофагеальной рефлюксной болезнью, которые были вовлечены в эти испытания из-за несовершенства критериев отбора больных. Однако мета-анализ G. Dopilla и соавт. (1989) показал, что при применении блокаторов Н2-рецепторов гистамина терапевтический эффект на 20% лучше по сравнению с плацебо. Существует мнение, что при функциональной диспепсии эффективной может оказаться высокая доза антагонистов Н2-рецепторов гистамина, но для подтверждения этого мнения необходимы серьезные клинические работы.
Ингибиторы протонной помпы практически не применялись при функциональной диспепсии. Недавно завершенное серьезное клиническое исследование с высокой статистической достоверностью продемонстрировало хороший эффект омепразола при функциональной диспепсии, причем лучший результат был получен в группе больных с язвенноподобным вариантом синдрома по сравнению с дискинетическим. В исследовании OCAY монотерапия омепразолом оказалась так же эффективна в купировании симптомов диспепсии, как и эрадикационная терапия инфекции H.pylori.
Противоречивые результаты получены при проведении эрадикационной терапии инфекции H.pylori при функциональной диспепсии: некоторые исследования показали улучшение клинической симптоматики после уничтожения H.pylori, некоторые исследования не получили заметного положительного эффекта после эрадикации. Исследование J. Gillvary и соавт. (1997) выделяется из ряда таких работ, так как в качестве эрадикационной схемы использовали классическую тройную терапию с субцитратом коллоидного висмута. Маастрихтский консенсус-II поставил точку в этой дискуссии и назвал функциональную диспепсию в качестве показания к эрадикационной терапии на основании следующих положений: эрадикация H.pylori является приемлемым выбором в тактике лечения функциональной диспепсии; у некоторой части больных эрадикация H.pylori приводит к длительному улучшению самочувствия.
Таким образом, этиотропное для хронического геликобактерного гастрита лечение помогает не всем больным функциональной диспепсией, что свидетельствует об отсутствии тождественности этих заболеваний и о неоднородности больных функциональной диспепсией. Вероятно, воспалительные изменения слизистой оболочки желудка не являются основной причиной диспептических симптомов.
Негеликобактерные гастриты
- Аутоиммунный гастрит
После широко распространенного геликобактерного гастрита наибольшее клиническое значение имеет аутоиммунный гастрит, ассоциированный с пернициозной анемией, который в Сиднейской системе помещен под рубрикой атрофического гастрита. При этом заболевании в 90% случаев обнаруживаются антитела к париетальным клеткам и к Н+,К+-АТФазе, в 60% случаев — антитела к фактору Касла, в 50% случаев- антитиреоидные антитела. Резко выраженная атрофия фундальных желез клинически проявляется ахилией, при этом характерна ответная гипергастринемия и гиперплазия G-клеток. Риск возникновения рака желудка на фоне аутоиммунного гастрита в 3-10 раз выше, чем в популяции.
- Особые формы гастрита
В Сиднейской системе к особым формам гастрита отнесены химический, радиационный и инфекционный гастриты, которые мы группируем по этиологическому признаку, и эозинофильный, лимфоцитарный и гранулематозный гастриты, которые мы группируем по их морфологическим особенностям и диагностике.
Это достаточно редкие заболевания, уступающие по своему клиническому значению хроническому геликобактерному гастриту, который благодаря изучению H.pylori мы можем сегодня успешно распознавать и лечить.
Литература 1. Аруин Л.И, Капуллер Л.Л., Исаков В.А. Морфологическая диагностика болезней желудка и кишечника. Москва, Триада-Х, 1998 г. 2. Ивашкин В.Т., Успенский В.М. Некоторые функциональные и гистохимические изменения в двенадцатиперстной кишке при язвенной болезни (по данным телеметрии и дуоденобиопсии). // Советская медицина, 1970, № 3, С. 10-14. 3. Ивашкин В.Т., Дорофеев Г.И. Нарушения резистентности слизистой оболочки желудка и двенадцатиперстной кишки при хроническом гастрите и язвенной болезни. // Советская медицина, 1983, № 2, С. 10-15. 4. Ивашкин В.Т. Эрадикация инфекции Helicobacter pylori и ремиссия язвенной болезни: однозначны ли эти состояния? // Российский журнал гастроэнтерологии, гепатологии и колопроктологии, 1999, Т.8, № 3, С. 71-73.